O uso generalizado de pequenos eletrodomésticos pelos consumidores implica a necessidade de fontes de energia, ou circuitos de alimentação única. células galvânicasAs baterias, também conhecidas como pilhas, surgiram em 1800, graças ao físico italiano Alessandro Volta. Elas variam em tamanho e formato, voltagem, capacidade e tipo. As pilhas alcalinas e salinas são amplamente utilizadas no mercado de pequenos eletrodomésticos e eletrônicos.
O que são baterias salinas?
Baterias de sal — fontes de corrente elétrica geradas em um dispositivo simples por meio de uma reação química. Às vezes são chamadas de baterias de carbono-zinco ou baterias de carbono. Este tipo de célula é considerado o mais barato, mas tem baixa densidade de energia, o que a torna adequada para dispositivos de baixa potência. Em dispositivos com alto consumo de energia ou com picos característicos de corrente de carga e temperatura, elas não duram muito e, portanto, não são utilizadas.
Designação de baterias de sal
A designação de baterias salinas é aceita de acordo com diversas normas:
- Sistema de classificação americano.
- Sistema internacional (IEC).
- Padrão interestadual (GOST).
| Sistema de classificação americano | Classificação Internacional IEC | GOST | Tamanho, mm | Capacidade, mAh |
| UM | R23 | 17x50 | ||
| AA | R6 | 316 | 14,5 x 50,5 | 1100 |
| AAA | R03 | 286 | 10,5 x 44,5 | 540 |
| C | R14 | 343 | 26,2x50 | 3800 |
| D | R20 | 373 | 34,2 x 61,5 | 8000 |
| F | R25 | 33x91 | ||
| 1/2AA | R$ 14.250 | 312 | 14,5x25 | 250 |
| R10 | R10 | 332 | 21,5 x 37,3 | 1800 |
Por exemplo, a marcação R 6 de uma bateria salina significa: redonda, cilíndrica, dedo, elemento do tipo sal, dimensões gerais 14,5x50,5, capacidade1100 mAh. A voltagem padrão é de 1,5 V. A designação "R" (sal) no rótulo da bateria distingue as baterias de solução salina de outros tipos de baterias (alcalinas ou de lítio).
Design e composição
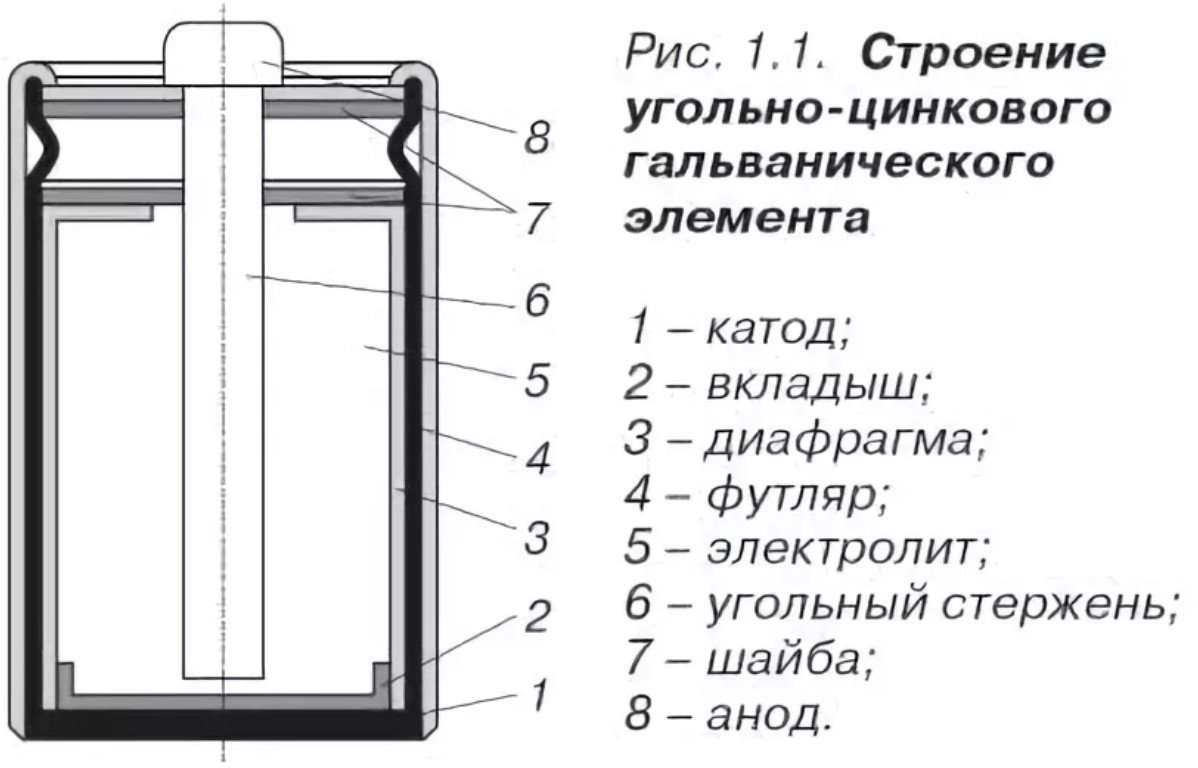
O projeto de uma bateria de sal é bastante simples e consiste em:
- Cátodo - o mesmo a caixa da bateria de sal é feita feito de zinco, com propriedades anticorrosivas aprimoradas e alto grau de pureza (menos).
- O ânodo é um aglomerado, fabricado por prensagem, impregnado com eletrólito (plus).
- Eletrólito: cloreto de amônio ou cloreto de zinco, com adição de um espessante (amido).
- Condutor de corrente de carbono - percorre o centro, tratado com composição de parafina.
- Câmara de gás - localizada na parte superior, projetada para coletar gases da reação química.
- A junta, localizada na parte superior, funciona como um vedante.
- Caixa protetora - de papelão ou lata - para proteger contra corrosão e vazamentos de eletrólitos.
Vamos considerar a composição de uma bateria salina do ponto de vista químico:
- O cátodo é feito de zinco altamente purificado, resistente à corrosão.
- Ânodo - Mistura de MnO2, grafite, impregnação eletrolítica.
- O eletrólito é cloreto de amônio ou uma mistura de cloreto de zinco com cloreto de cálcio.
Quais baterias são melhores: salinas (1) ou alcalinas (2)?
A comparação pode ser feita na forma de uma tabela, onde as vantagens e desvantagens dos diferentes tipos de elementos ficam claramente visíveis:
| Parâmetros de comparação | 1 | 2 |
| Condições de temperatura, condições de operação | O desempenho é reduzido em baixas temperaturas e não suporta picos de corrente. | Funciona bem em baixas temperaturas - até -20°C.OResistem facilmente a picos de tensão e não temem aumentos repentinos na corrente de carga. |
| Consumir antes de: | 2 a 3 anos | 5 anos |
| Aplicativo | Adequado para uso em dispositivos com baixo consumo de corrente. | Adequado para uso em equipamentos com consumo de energia médio e alto. |
| Instrumentos, dispositivos técnicos | Despertadores, relógios de parede, controles remotos, mini lanternas, brinquedos simples | Aparelhos de reprodução, lanternas, brinquedos musicais, gravadores de voz, monitores de pressão arterial |
Ao escolher uma fonte de energia para um dispositivo com requisitos operacionais específicos, é importante saber como distinguir entre uma pilha salina e uma pilha alcalina. Enquanto as pilhas salinas são marcadas com a letra R, as pilhas alcalinas são precedidas pela letra L (LR).
Conclusões e recomendações
Este tipo de fonte de energia é mais leve e acessível. No entanto, a vida útil das baterias de solução salina é curta — de 2 a 3 anos — e elas podem sofrer autodescarga parcial durante o armazenamento e durante o uso, em caso de pico repentino de corrente. Portanto, dado o seu desempenho relativamente fraco, mas o seu custo relativamente baixo, é fácil adquirir vários conjuntos de baterias como reserva.
Não é alto capacidadeAs baterias de sal (2 a 3 vezes menos potentes que outros tipos) limitam seu uso a dispositivos simples com baixa corrente de carga.
É fácil determinar se é possível carregar baterias de solução salina: o nome da bateria está indicado no corpo do dispositivo destinado ao carregamento. capacidadeEm mAh. Se esse valor não estiver disponível, trata-se de uma pilha comum e, apesar de inúmeros especialistas recomendarem, não se deve carregá-la. Carregá-la não proporcionará o efeito esperado a longo prazo e pode causar acidentes devido ao superaquecimento e vazamento do eletrólito. Se você precisa de uma fonte de energia mais confiável e duradoura, é melhor investir em uma pilha alcalina ou recarregável.
Curiosidade: bateria de sal faça você mesmo É muito simples de fazer. Você vai precisar de moedas de 50 kopeks, papel alumínio, papel-moeda e uma solução salina. É melhor mergulhar as moedas em uma solução de vinagre antes de usar para remover qualquer placa ou sujeira. Monte o dispositivo: uma moeda, papel-moeda embebido na solução salina e papel-moeda. Repita esse processo várias vezes, criando uma coluna com a moeda (positivo) em uma extremidade e o papel-moeda (negativo) na outra. A corrente é gerada pela diferença de potencial criada pelo eletrólito (solução salina) entre o metal do papel-moeda e a moeda. Essa invenção é chamada de pilha voltaica, e sua voltagem depende diretamente do número de moedas usadas: quanto mais moedas, maior a voltagem obtida. No entanto, após o experimento, as moedas não serão mais utilizáveis; elas ficarão com uma camada de ferrugem.